Введение
В настоящее время сахарный диабет (СД) продолжает оставаться одним из наиболее распространенных неинфекционных заболеваний во всем мире. Ожидаемое число пациентов, страдающих СД к 2045 г. может составляь 343 млн (Diabetes Atlas, 2021). Более того, гипергликемия во время беременности выявлена у 21 млн женщин, и 80% из них имели именно гестационный СД (ГСД). Таким образом, на сегодняшний день каждые 6-е роды происходят от беременности, протекавшей на фоне ГСД [1].
Следует напомнить, что ГСД представляет собой заболевание, которое характеризуется впервые выявленной гипергликемией именно во время беременности, но не соответствующей критериям манифестного СД [2]. Безусловно, ГСД представляет крайне серьезную угрозу здоровью как матери, так и плода ввиду наличия риска развития таких осложнений, как преэклампсия, макросомия, родовые травмы, неонатальные гипогликемии, а также мертворождение [3]. Более того, ГСД является фактором риска развития в будущем ряда патологий, таких как ожирение, СД 2 типа (СД2) и сердечно-сосудистые заболевания у матери и потомства [1, 3]. Таким образом, доказано, что ГСД представляет собой крайне актуальную проблему для современной медицины.
Современные методы терапии ГСД, направлены прежде всего на предупреждение чрезмерного роста плода и развития осложнений. Согласно актуальным представлениям, всем беременным с ГСД необходима модификация образа жизни и диетотерапия. В рационе рекомендуется исключить легкоусваиваемые углеводы и транс-жиры.
Рекомендованное суточное количество углеводов должно составлять 175 г, или не менее 40% от расчетной суточной калорийности питания. под обязательным контролем гликемии, а также наличия кетоновых тел в моче. Углеводсодержащие продукты целесообразно распределять на 3 основных приема пищи в течение дня с 2–3 дополнительными перекусами. Каждый основной прием пищи должен включать медленноусваиваемые углеводы, белок, моно- и полиненасыщенные жиры, пищевые волокна. В случае наличия у беременной ожирения рекомендовано ограничить в рационе насыщенные жиры до 10% от суточной нормы, а калорийность рациона должна составлять не менее 1800 ккал/сут. для предотвращения появления кетонурии.
В случае невозможности достижения целевых значений гликемии в течение 1–2 недель пациенткам требуется назначение инсулинотерапии. Следует отметить, что потребность в инсулине у всех пациентов разная и дозы инсулина подбираются индивидуально. Старт инсулинотерапии проводится с малых доз с последующей̆ титрацией. При превышении допустимого уровня глюкозы в цельной капиллярной крови через 1 час после начала приема пищи – инициация терапии болюсным инсулином, в случае повышения гликемии натощак – инициация терапии базальным инсулином. Титрация дозы проводится каждые 3 дня с увеличением на 1–2 ЕД до достижения целевых значений гликемии [4].
Однако на сегодняшний день при соблюдении рекомендаций по лечению далеко не всегда получается добиваться желаемого эффекта. В связи с этим можно предположить, что вопрос выбора терапии ГСД зависит от ряда факторов. Одним из важнейших факторов, определяющих эффективность немедикаментозной терапии и необходимость назначения инсулинотерапии, вероятно, являются патофизиологические механизмы формирования гипергликемии во время беременности.
В настоящее время ряд исследований продемонстрировал, что дефект секреции инсулина или чувствительности к нему, по всей вероятности, играют ведущую роль в развитии ГСД у беременных, что позволяет выделять различные подтипы заболевания [5]. Так, в 2016 г. C. Powe et al. в работе «Heterogeneous Contribution of Insulin Sensitivity and Secretion Defects to Gestational Diabetes Mellitus» на группе беременных женщин (809 человек) продемонстрировали, что в основе ГСД могут лежат как дефекты чувствительности к инсулину с гиперинсулинемией, так и дефекты секреции инсулина при нормальной чувствительности к нему (1/3 женщин) [6].
В 2018 г. в процессе изучения влияний различных подтипов ГСД на перинатальные исходы Y. Liu et al. выделили 3 подтипа ГСД: с преобладанием ИР, с преобладанием дисфункции β-клеток, а также смешанный тип (оба признака выражены равнозначно) [7]. Схожие результаты в 2019 г. получены M. Feghali et al. в исследовании «Subtypes of gestational diabetes mellitus based on mechanisms of hyperglycemia», также описаны патофизиологические механизмы с дефектом β-клеток поджелудочной железы, преобладанием ИР или сочетанием этих факторов, что также позволило выделить 3 подтипа ГСД [8].
Однако наиболее большое значение представляет исследование «Characteristics and pregnancy outcomes across gestational diabetes mellitus subtypes based on insulin resistance», выполенное K. Benhalima et al., проведенное в 2019 г., куда были включены 1813 беременных женщин. Помимо описания клинической характеристики подтипов ГСД в зависимости от выраженности ИР впервые была оценена эффективность проводимой терапии данных подтипов. И оказалось, что, несмотря на различные патологические механизмы, различий в потребности в инсулинотерапии, среди пациенток с ГСД и различными подтипами обнаружено не было [9].
Таким образом, принимая во внимание данные исследований последних лет, можно смело говорить о выделении различных подтипов ГСД, исходя из преобладания патологического механизма либо дефекта β-клеток, либо ИР, или комбинации этих факторов [6–9]. Выявление различных подтипов ГСД может иметь крайне большое клиническое значение, поскольку от механизмов, лежащих в основе патогенеза нарушений углеводного обмена, может зависеть выбор тактики лечения пациенток и как результат – достижение ими целевых значений глюкозы в крови с учетом того, что необходимо оценить эффективность современных методов лечения, таких как дието- и инсулинотерапия, в зависимости от подтипа ГСД.
Цель исследования: оценить эффективность современных методов лечения в зависимости от подтипа ГСД.
Методы
Клиническая часть исследования, одобренного локальным независимым этическим комитетом (Протокол № 5/21 от 11.03.2021), выполнена на базе кафедры внутренних болезней № 3, Научно-исследовательского института акушерства и педиатрии ФГБОУ ВО РостГМУ Минздрава РФ. Исследование проводилось с апреля 2021 по август 2022 г.
В данное наблюдательное проспективное исследование были включены 130 беременных на сроке 24–28 недель в возрасте 18 лет и старше вне зависимости от факторов риска ГСД, средний возраст которых составил 30,2 (27–33) года. Все беременные, включенные в исследование, не прибегали к проведению вспомогательных репродуктивных технологий, не страдали какими-либо нарушениями углеводного обмена до беременности и не принимали сахароснижающих препаратов.
Диагноз ГСД был подтвержден на основании перорального глюкозотолерантного теста (ПГТТ) с 75 г глюкозы с дополнительным определением значений инсулина натощак также через 1 и 2 часа после нагрузки для определения индекса ИР Matsuda, на основании которого проводилось определение подтипа ГСД [10–13]. Расчет выполнялся по формуле ISI (MATSUDA)=10,000/√(G0хI0х(GmeanхImean), где ISI – индекс Matsuda, I0 – концентрация инсулина в плазме натощак, G0 – концентрация глюкозы в плазме натощак, Gmean – средняя концентрация глюкозы в плазме крови во время ПТГТ, Imean – средняя концентрация инсулина в плазме крови во время ПГТТ, 10,000 – упрощающая константа для получения чисел от 0 до 12, √ – исправление распределения нелинейных значений.
Все лабораторные показатели определяли в венозной плазме, индексы – расчетным методом. При индексе Matsuda менее 50-го процентиля от значения беременных без ГСД говорили о превалировании процессов ИР, при более 50-го процентиля – о дисфункции β-клеток. В зависимости от преобладающего патогенетического механизма сформированы следующие группы пациенток: группа I – 45 беременных с ГСД и нарушением функции β-клеток, группа II – 43 беременные с ГСД и ИР.
В ходе настоящего исследовали оценены варианты получаемого лечения и их эффективность по уровню достижения целевых значений гликемии. У всех пациенток были изучены особенности пищевого рациона на основе специально разработанной анкеты. После выявления ГСД всем беременным назначена диетотерапия, которая включала суточное количество углеводов 175 г, или не менее 40% от расчетной суточной калорийности питания, углеводсодержащие продукты, распределенные на три основных приема пищи в течение дня с 2–3 дополнительными перекусами. У беременных, которые получали инсулинотерапию, были оценены схемы введения инсулина: болюсная, базальная и базис-болюсная. В качестве болюсного инсулина использовался инсулин аспарт, базального – инсулин детемир. Оценка эффективности лечения проводилась по результатам самоконтроля глюкозы крови глюкометром, целевыми значениями считались уровень глюкозы крови натощак до 5,1 ммоль/л, через 1 часа после приема пищи – до 7,0 ммоль/л.
Статистический анализ результатов исследования проведен с использованием R (версия 3.2, R Foundation for Statistical Computing, Vienna, Austria). Сравнение количественных показателей в группах проведен с помощью теста Краскала–Уоллиса (попарные апостериорные сравнения производились с помощью метода Неменьи), частот – с помощью точного теста Фишера с поправкой на множественные сравнения по Холму. Данные считались статистически значимыми при р<0,05. Данные приведены в виде медиан и интерквартильных интервалов количественных показателей в группах.
Результаты
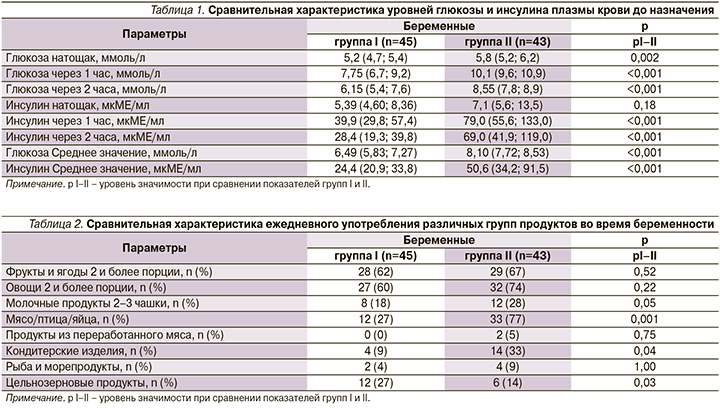
В ходе исследования проанализированы уровни глюкозы и инсулина плазмы крови до лечения. Оказалось, что в группе ГСД и ИР показатели глюкозы крови натощак, через 1 и 2 часа после ПГТТ были статистически значимо выше, чем в группе ГСД и дефектом β-клеток (р<0,001). Кроме того, более высокие уровни инсулина плазмы крови через 1 и 2 часа также отмечались в группе ГСД и ИР по сравнению с группой ГСД и дефектом β-клеток (р<0,001). В то же время уровень инсулина плазмы крови натощак статистически значимо между группами не различался (р=0,18). Сравнительная характеристика уровней глюкозы и инсулина плазмы крови до назначения лечения представлена в табл. 1.
Далее были изучены получаемые методы лечения пациенток с различными подтипами ГСД. Следует отметить, что у всех пациенток в зависимости от полученного лечения достигнуты целевые значения уровня глюкозы крови по данным самоконтроля, что говорит об эффективности их применения.
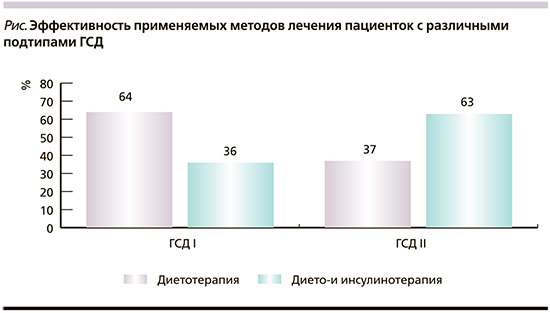
В группе ГСД и дефектом β-клеток 29 (64,4%) пациенток получали только немедикаментозную терапию, в то время как 16 (35,6%) беременных использовали диетотерапию совместно с введением инсулина. Следует отметить, что среди 16 пациенток, получавших оба варианта лечения, 9 (56,3%) беременным вводили только базальный инсулин, 6 (37,5%) больным – болюсный и лишь 1 (6,2%) пациентка применяла базис-болюсный режим инсулинотерапии.
В группе ГСД и ИР всего 16 (37,2%) пациенток получали только немедикаментозную терапию, тогда как 27 (62,8%) беременных использовали диетотерапию совместно с инсулинотерапией. В то же время среди 27 пациенток, получавших оба варианта лечения, 13 (48,1%) беременным вводили только базальный инсулин, 12 (44,5%) – болюсный и лишь 2 (7,4%) пациентки применяли базис-болюсный режим инсулинотерапии. Таким образом, пациентки с ГСД и дефектом β-клеток статистически значимо реже получали инсулинотерапию по сравнению с беременными в группе ГСД и ИР: 16 (35,6%) человек против 27 (62,8%), р=0,04 (см. рисунок).
Отдельно следует отметить диетотерапию, которую получали пациентки обеих групп, поскольку были выявлены значительные различия по потреблению разных групп продуктов. Так, в группе ГСД и ИР значимо больше беременных употребляли мясные продукты (мясо/птица/яйца) относительно группы ГСД с дефектом β-клеток: 33 (77%) человек против 12 (27%), р=0,001. В то же время пациентки в группе ГСД и ИР значительно реже использовали в рационе цельнозерновые продукты по сравнению с беременными группы ГСД и дефектом β-клеток: 6 (14%) человек против 12 (27%), р=0,03. Отдельный интерес вызывает тот факт, что в группе ГСД и ИР, несмотря на рекомендованные ограничения, значимо больше беременных употребляли кондитерские изделия относительно группы ГСД и с дефектом β-клеток: 14 (33%) человек против 4 (9%), р=0,04. Сравнительная характеристика ежедневного употребления различных групп продуктов представлена в табл. 2.
Обсуждение
Полученные данные позволяют говорить о том, что фактический рацион беременных с различными подтипами ГСД не имел значительных различий. Представленные результаты демонстрируют, что большее число беременных с ГСД и ИР относительно беременных с дисфункцией β-клетки употребляют ежедневно мясные продукты и кондитерские изделия. С другой стороны, представленные данные позволяют говорить о том, что больше беременных с ГСД и дисфункцией β-клеток относительно беременных с ГСД и ИР ежедневно употребляют цельнозерновые продукты.
Отдельно следует отметить результаты, указывающие на эффективность возможных методов лечения при различных подтипах ГСД. Несмотря на разочаровывающие результаты в работе K. Benhalima et al. в 2019 г., не продемонстрировавшие различий в выборе метода лечения, в нашей работе пациентки с ГСД и дисфункцией β-клеток чаще достигали компенсации ГСД на фоне только немедикаментозного лечения, что может быть связано со снижением уровня инсулина у беременных, число которого при ограничении употребления углеводов оказалось достаточным для достижения целевых значений. В то время как пациенткам с ГСД и ИР достичь целевых значений уровня глюкозы чаще удавалось при инсулинотерапии, что, вероятно, связано с выраженностью ИР, которую не удается преодолевать без введения высоких доз инсулина и как следствие – добиваться снижения гликемии.
Представленные результаты позволяют говорить о том, что для беременных с ГСД и дисфункцией β-клеток диетотерапия наиболее эффективна и должна рассматриваться как первый этап терапии. На втором этапе, через 1–2 недели в отсутствие эффекта, согласно клиническим рекомендациям, следует добавить инсулинотерапию. Однако для беременных с ГСД и ИР может быть рассмотрено назначение совместно и диетотерапии, и инсулинотерапии на первом же этапе, не выжидая эффекта от коррекции режима питания в течение 2 недель.
Заключение
В настоящее время определение различных подтипов ГСД может иметь крайне большое клиническое значение, поскольку от механизмов, лежащих в основе патогенеза нарушений углеводного обмена, могут зависеть выбор тактики и своевременность назначения лечения беременным с ГСД, как результат – улучшение прогноза данных.
Были изучены современные методы лечения в зависимости от подтипа ГСД, а именно их эффективность. Оказалось, что пациентки с ГСД и дисфункцией β-клеток чаще достигают компенсации ГСД на фоне только немедикаментозного лечения, в то время как пациенткам с ГСД и ИР чаще требуется инсулинотерапия. Следовательно, для беременных с ГСД и дисфункцией β-клеток диетотерапия наиболее эффективна и должна рассматриваться как первый этап терапии. На втором этапе через 1–2 недели в отсутствие эффекта следует добавлять инсулинотерапию. В то время как для беременных с ГСД и ИР наиболее эффективно на первом этапе сразу применять инсулинотерапию.
Таким образом, полученные данные, которые безусловно требуют дальнейшего изучения, могут стать основой для разработки нового персонализированного подхода к ведению пациенток с ГСД в дополнение к уже имеющимся алгоритмам, но в зависимости от конкретного подтипа ГСД, что в свою очередь позволит существенно снижать риски неблагоприятных исходов беременности и дальнейшей непереносимости глюкозы в послеродовом периоде.
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы: «Различные подтипы гестационного сахарного диабета: патогенез, клиническая характеристика, диагностические критерии, особенности лечения».



