Обоснование
Сахарный диабет 2 типа (СД2) характеризуется высокой распространенностью, значительным риском развития макро- и микрососудистых осложнений, существенным неблагоприятным влиянием на прогноз [1, 2]. Среди ассоциированных с СД2 нарушений функциональные изменения со стороны кишечника, в т.ч. синдром раздраженного кишечника (СРК), являются недостаточно изученной проблемой [3]. Сообщается, что до 15–35% больных СД2 имеют различные типы СРК [4]. В развитии нарушений кишечного (в частности, толстокишечного) транзита у лиц с СД2 важную роль отводят диабетической вегетативной невропатии, развитие которой связывают с феноменами инсулинорезистентности, глюко- и липотоксичности и накопления в тканях конечных продуктов гликирования [5]. У больных обсуждаемой категории остаются неустановленными такие клинико-анамнестические особенности СРК, как распределение его на варианты, макроскопические и гистологические характеристики слизистой оболочки толстого кишечника, определяемые при инструментальных исследованиях, а также спектр факторов, провоцирующих развитие симптоматики СРК [6].
Цель исследования: проспективное изучение клинико-анамнестических особенностей больных СРК в сочетании с СД2 по сравнению с лицами с СРК без диабета.
Методы
Под наблюдением находились 107 больных, из них 42 (39,3%) мужчины и 65 (60,7%) женщин в возрасте от 36 до 66 лет (средний возраст – 48,9±9,4 года) с СД2 и наличием клинических проявлений СРК. Кроме того, наблюдались 52 больных СРК без диабета, из них 21 (40,4%) мужчина и 31 (59,6%) женщина (средний возраст – 43,7±6,8 года), различий по полу и возрасту между этими группами не было (р>0,05). Среди лиц с СД2 давность диабета составила 6,9±2,6 года, средний уровень гликированного гемоглобина (HbА1с) – 7,93±0,51%. Диагноз СД2 и его осложнений устанавливали на основании рекомендаций Российской Ассоциации эндокринологов [7]. Диагноз СРК рассматривали как диагноз исключения и устанавливали у всех больных на основании Римских критериев IV пересмотра [8]. Особое внимание в процессе диагностики уделяли исключению органических поражений кишечника, для чего учитывали стандартные «симптомы тревоги» и проводили клинико-лабораторные и инструментальные исследования в соответствии с отечественными и международными рекомендациями: общий анализ крови, С-реактивный белок, общий анализ кала, тест на скрытую кровь, ультразвуковое абдоминальное исследование, фиброгастродуоденоскопия, фиброколоноскопия (ФКС) с биопсией слизистой оболочки толстой кишки (в 54 случаях, включая 30 лиц с СД2 и 24 – без диабета), выявление антител к глиадину, тканевой трансглютаминазе (в 33 наблюдениях, включая 19 лиц с СД2 и 14 – без диабета) и др. [9]. В соответствии с Клиническими рекомендациями Российской гастроэнтерологической ассоциации и Ассоциации колопроктологов России, выделяли следующие варианты СРК: с диареей (СРК-Д), с запорами (СРК-З), неклассифицируемый (СРК-Н) и смешанный (СРК-М) [9].
У всех больных СРК оценивали жалобы и анамнез, проводили стандартное объективное исследование. При анализе жалоб характеризовали наличие и особенности таких клинических проявлений СРК, как диарея (выраженность, связь с временем суток, приемом пищи), запоры, абдоминальная боль (с установлением ее локализации, интенсивности, характера, связи с эмоциональными факторами, приемом пищи, актом дефекации), вздутие, также учитывали жалобы со стороны верхних отделов желудочно-кишечного тракта (ЖКТ), включая тошноту, рвоту, чувство раннего переполнения в эпигастрии, отрыжку кислым [10]. Степень выраженности клинических проявлений СРК устанавливали по опроснику GSRS (Gastrointestinal Symptom Rating Scale) [11]. Особое внимание обращали на установление таких особенностей анамнеза, как малоподвижный образ жизни, данные о психоэмоциональном стрессе в дебюте и в ходе развития симптоматики СРК, наличие повышенной тревожности (по данным консультаций невролога, психиатра), курения, гипотиреоза, хронической обструктивной болезни легких, приема в дебюте СРК антибиотиков и нестероидных противовоспалительных средств (НПВС), сведения о перенесенной инфекции COVID-19, а также данные семейного анамнеза.
Для обработки данных использовали программу Microsoft Excel, 2007. Описательные характеристики представлены в виде средних±стандартное отклонение (М±SD); категориальные данные представлены в виде процентов (%). Для оценки степени статистической достоверности различий использовали t-критерий Стьюдента, достоверность во всех случаях устанавливали при величинах р<0,05 [12].
Результаты
При анализе вариантов СРК отмечено достаточное сходство их распределения между группами с наличием и отсутствием СД. Так, у лиц как с СД2, так и без диабета наиболее распространенным был СРК-Д – 49 (45,8%) и 30 (57,6%) случаев соответственно, несколько реже был представлен СРК-З – 36 (33,6%) и 16 (30,8%) соответственно, существенно меньшими были доли лиц с СРК-М – 13 (12,2%) и 3 (5,8%) соответственно и с СРК-Н – 9 (8,4%) и 3 (5,8%) соответственно. В то же время среди лиц с СРК с СД2 отчетливо выше, чем у больных СРК без диабета, оказались доли тех, кто имел варианты СРК-Д и СРК-М (различия в распределении достоверны, р<0,05).
Схожими оказались также данные ФКС с биопсией слизистой оболочки толстой кишки, которая была выполнена 54 больным СРК (включая 30 лиц с СД2 и 24 – без диабета). Во всех случаях показаниями к ее проведению стала необходимость исключения органических поражений кишечника в процессе дифференциальной диагностики СРК. В подавляющем большинстве случаев у обследованных лиц имела место нормальная макроскопическая картина слизистой оболочки кишечника – 22 (73,3%) случая в группе СРК с СД2 и 14 (58,3%) – СРК без диабета в отсутствие гистологических отклонений от нормы: соответственно 19 (63,3%) и 17 (62,9%), причем между группами с СД и без него различий в особенностях макро- и микроскопической картины слизистой оболочки толстого кишечника выявлено не было. Так, умеренная гиперемия слизистой оболочки кишечника имела место в 5 (16,7%) случаях среди лиц с СРК с СД2 и у 7 (29,2%) – с СРК без диабета, поверхностные катаральные изменения – в 3 (10,0%) и 4 (16,7%) наблюдениях соответственно, незначительная отечность стенки и наложения слизи – в 2 (6,7%) и 5 (20,8%), гиперплазия бокаловидных клеток – в 8 (26,6%) и 6 (25,0%), незначительная клеточная инфильтрация – в 2 (6,7%) и 3 (12,5%), увеличение числа фибробластов стромы – в 6 (20,0%) и 7 (29,2%) (р>0,05). Все перечисленные как макро-, так и микроскопические изменения слизистой оболочки, выявленные у обследованных больных, могут присутствовать при СРК и характеризуются авторитетными источниками как неспецифические [13].
В табл. 1 показана сравнительная характеристика жалоб со стороны ЖКТ, которые предъявляли лица с СРК, включая пациентов как с СД2, так и без диабета.
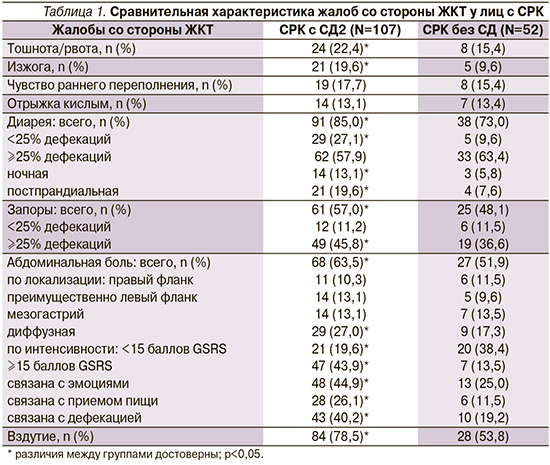
Клиническая картина СРК у лиц с СД2 по сравнению с пациентами без СД характеризовалась более высокой распространенностью диареи, запора, абдоминальной боли и вздутия, а также более значительной выраженностью диареи, более высокими долями ночной и постпрандиальной диареи, большей выраженностью запоров и интенсивностью абдоминальной боли, отчетливо более высокой частотой связи абдоминальной боли с эмоциональным фактором, приемом пищи и с актом дефекации.
Табл. 2 иллюстрирует особенности анамнеза у больных СРК с СД2 по сравнению с СРК при отсутствии диабета.
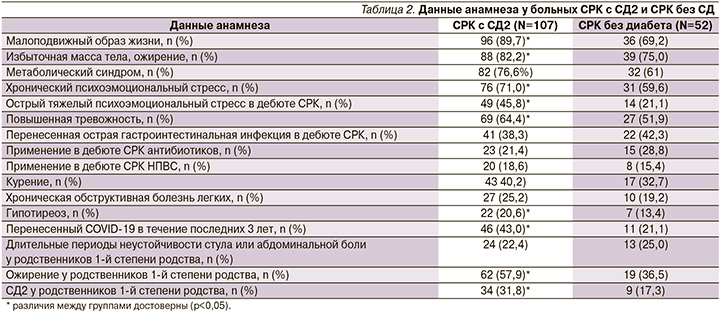
Отметим, что в обеих группах весьма высокими оказались доли больных, которые вели малоподвижный образ жизни (таких оказалось более 2/3 в каждой из групп), имели избыточную массу тела, ожирение или метаболический синдром (их было не менее 3/4 от общего числа), часто имели хронический психоэмоциональный стресс (более 1/2). В дебюте СРК у многих были представлены острый тяжелый психоэмоциональный стресс (около 1/3 случаев), острые гастроинтестинальные инфекции (также около 1/3), несколько реже отмечали прием антибактериальных средств (не менее 1/5) и НПВС (1/6 часть наблюдений). Существенной была распространенность в обеих группах курения (около 1/3), перенесенной в течение последних 3 лет инфекции CОVID-19 (также примерно у 1/3), гипотиреоза (1/6–1/5 случаев) и наличия в семейном анамнезе длительных периодов неустойчивости стула или абдоминальной боли у родственников 1-й степени родства (около 1/4). При сравнении выделенных групп между собой отмечено, что среди больных СРК с СД2 по сравнению с лицами с СРК без диабета статистически значимо более высокими оказались доли тех, кто вел малоподвижный образ жизни, имел избыточную массу тела, ожирение или метаболический синдром (р<0,05). Пациенты с СД2 чаще имели психоэмоциональные проблемы в анамнезе, включая хронический психоэмоциональный стресс, острый тяжелый психоэмоциональный стресс в дебюте СРК и повышенную тревожность (р<0,05). Также большое значение имели гипотиреоз, перенесенная в течение последних 3 лет инфекция CОVID-19, ожирение и СД2 у родственников 1-й степени родства в семейном анамнезе (р<0,05).
Данные оценки особенностей анамнеза у лиц с СД2, имевших разные варианты СРК, представлены в табл. 3.
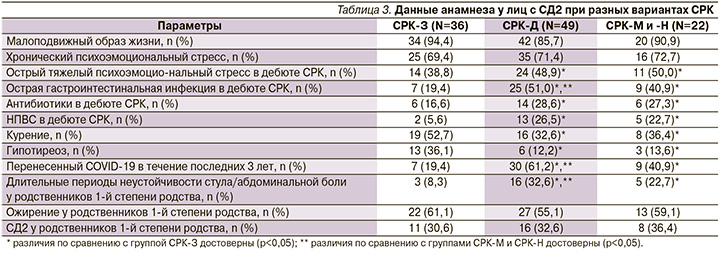
Как видно из табл. 3, имели место статистически достоверные различия между выделенными группами по ряду параметров. Так, у лиц с СРК-Д, а также с СРК-М и СРК-Н статистически значимо выше, чем при СРК-З, оказались доли больных, у которых в дебюте кишечных нарушений были представлены острый тяжелый психоэмоциональный стресс (р<0,05), острая гастроинтестинальная инфекция (р<0,05), прием антибиотиков (р<0,05) и НПВС (р<0,05).
В группах СРК-Д, СРК-М и СРК-Н были выше, чем при СРК-З, доли лиц, ранее перенесших инфекцию COVID-19 и имевших длительные периоды неустойчивости стула или абдоминальной боли у родственников 1-й степени родства, р<0,05. В то же время у лиц с СРК-З достоверно выше, чем при других вариантах СРК, были доли лиц, имевших в анамнезе курение и гипотиреоз, р<0,05. Больные СРК-М и СРК-Н в отношении анализируемых данных анамнеза нередко представляли промежуточное отношение между лицами с СРК-Д и СРК-М.
Обсуждение
Сочетание СД2 и СРК представляет одну из недостаточно изученных проблем внутренних болезней [14]. Полученные в настоящей работе данные позволяют говорить о сходстве лиц с СРК с наличием диабета и без такового по распределению на клинические варианты СРК и по особенностям, выявляемым при ФКС с биопсией слизистой оболочки толстого кишечника. В то же время между этими группами больных отмечен ряд существенных различий по степени выраженности и особенностям клинических проявлений СРК, что может отражать влияние диабета на избыточную болевую чувствительность структур стенки кишечника и изменения кишечной моторики [15]. Возможно также, что наряду с локальным повышением готовности этих структур к развитию функциональных нарушений при СРК у лиц с диабетом также увеличивается восприимчивость к внешним стимулам (таким, как эмоциональный стресс, перенесенные инфекции, прием препаратов) и других компонентов оси «микробиота–кишечник–мозг» [16]. Все ее составляющие (включая микробиоту кишечника, энтеральную нервную систему, в т.ч. миэнтеральные сплетения Ауэрбаха и подслизистые сплетения Мейснера, симпатические и парасимпатические отделы вегетативной нервной системы, гипоталамо-питуитарно-надпочечниковую систему, нейроиммунные и нейроэндокринные системы, а также центральную нервную систему) у лиц с СД2 подвергаются воздействию присущих диабету метаболических нарушений, что может способствовать как усилению, так и видоизменению симптоматики СРК с формированием ряда клинических особенностей [17]. Таковыми, в частности, могут являться и обнаруженные при диабете более значительная выраженность симптомов СРК и более высокая распространенность ночной и постпрандиальной диареи, более тесная ассоциация абдоминальной боли с эмоциональным фактором, приемом пищи и с актом дефекации.
Анализ особенностей анамнеза лиц с СРК с наличием и отсутствием диабета также позволил установить наличие у них ряда значимых особенностей. Обращает на себя внимание важная роль психоэмоциональных травмирующих факторов в развитии клинических проявлений СРК у обсуждаемой категории лиц. Это в особенности важно для Донецкого региона, где выраженные психоэмоциональные перегрузки (обусловленные вынужденной миграцией, разлукой с близкими или их потерей, бытовыми и экономическими сложностями, ранениями, длительным пребыванием в районах, близких к линии боевого соприкосновения и др.) приходится испытывать значительному числу населения. Роль психоэмоциональных факторов в становлении симптомов СРК достаточно хорошо известна, однако у обследованного контингента лиц имелся ряд особенностей, включая как особые условия проживания в обстановке длительного гражданского конфликта, так и наличие СД2. В совокупности оба эти фактора в тесном взаимодействии усугубляли негативные эффекты друг друга и повышали риск более тяжелого течения СРК [17].
Несомненно, важную роль в развитии СРК у лиц с СД2 играли и эпизоды перенесенной острой гастроинтестинальной инфекции. Достаточная значимость этого пускового механизма СРК широко известна, ряд авторов выделяют и т.н. пост-инфекционную форму СРК [17]. Считают возможным, что развивающееся при острых кишечных инфекциях повышение проницаемости стенки кишечника приводит к транслокации комменсальных бактерий через эпителиальный барьер, что в свою очередь индуцирует развитие повреждения структур кишечной стенки и служит основой для формирования хронических нарушений ее функционирования у предрасположенных лиц [17]. Активно обсуждается роль при СРК синдрома избыточного бактериального роста. Его чаще выявляют при СРК-Д, однако и при СРК-З он выявляется более часто, чем у лиц без СРК [17]. Отметим, что если постинфекционная форма СРК в общей популяции лиц встречается примерно в 10% случаев, то у лиц с СРК и СД2 на связь с острой гастроинтестинальной инфекцией в дебюте СРК указывали от 19% больных СРК-З до 51% с СРК-Д. Столь высокие доли таких лиц могут свидетельствовать о дополнительной неблагоприятной роли диабета в реализации связанного с перенесенной инфекцией локального субклинического иммуновоспалительного процесса в стенке кишечника у этих больных [17].
Установленные связи симптоматики СРК с приемом антибиотиков и НПВС весьма показательны [17]. Все эти факторы признаются весомыми в развитии СРК и у лиц без диабета, однако у больных СД2 степень их негативного влияния на кишечную микробиоту, энтеральную нервную систему, а также гормональные механизмы может быть существенно более высокой по сравнению с пациентами без диабета [18].
Весьма показательны неблагоприятные эффекты курения на клинические проявления СРК. Табакокурение является одной из ведущих причин смерти в мире, важным фактором риска развития и прогрессирования сердечно-сосудистых и почечных поражений [18]. Многообразные неблагоприятные эффекты сопряжены также с пассивным курением. Негативно влияет на легочный и сердечно-сосудистый риск использование е-сигарет, мини-кальянов (вейпинг), изделий из нагреваемого табака (айкос), травяных смесей (спайс) [18]. Отказ от курения обеспечивает ряд благоприятных эффектов (часть из них развивается быстро, часть – замедленно до нескольких лет). Представлены данные, что при отказе от курения замедляется прогрессирование макро- и микрососудистых осложнений СД2 [18]. Полученные в настоящей работе данные о связи клинических проявлений СРК с курением свидетельствуют о существенном негативном влиянии этого фактора, отчетливо усугубляющем воздействие ассоциированных с диабетом патофизиологических механизмов [18].
Определенную значимость имеет отмеченная в работе связь клинических проявлений СРК с перенесенной инфекцией COVID-19. Известно, что люди с диабетом и ожирением не только более склонны к развитию тяжелых форм этой инфекции, но у них также чаще развивается постковидный синдром (по данным различных исследователей, диарея может присутствовать у 50–60% лиц с постковидным синдромом, запор – у 15–20%) [18]. β-клетки поджелудочной железы являются одной из мишеней для вируса SARS-CoV-2, что представляется важным фактором как ухудшения контроля гликемии у лиц с уже имеющимся диабетом в ходе развития COVID-19, так и формирования СД2 de novo в ходе этой инфекции [18]. С другой стороны, наличие диабета ассоциировано с рядом нарушений, включая центральное ожирение (и сопровождающее его хроническое воспаление), гиперкоагуляцию, сердечно-сосудистые заболевания, поражение почек. В совокупности все это может усугублять течение как респираторных, так тромбоэмболических и системных проявлений COVID-19 и в результате ухудшать прогноз [18]. Перенесенная инфекция COVID-19 представляет весомый фактор, провоцирующий ухудшение течения ряда хронических заболеваний внутренних органов, в т.ч. СРК, в особенности при его ассоциации с СД2 [19].
Отдельного рассмотрения заслуживает и отмеченная в работе связь клинических проявлений СРК (в частности, запора) у лиц с СД2 в сочетании с гипотиреозом, который среди наблюдавшихся больных отмечен в 20,6% случаев. С одной стороны, склонность к запорам является одной из известных особенностей лиц с гипотиреозом, но с другой – известно, что гипотиреоз вследствие аутоиммунного тиреоидита является наиболее частым сопутствующим нарушением при диабете [19]. Отмеченная в настоящей работе частота встречаемости гипотиреоза у лиц с СД2 соответствует таковой в литературных источниках для этой категории лиц [19]. В то же время воздействие этого сопутствующего состояния на клиническую картину СРК представляет собой относительно малоизученный момент. Несомненно, что адекватная коррекция нарушения функции щитовидной железы у таких больных способна благоприятно влиять на симптоматику СРК, а возможно, и дополнительно благоприятно воздействовать и на контроль диабет-ассоциированных метаболических нарушений и течение осложнений СД2 [20].
Заключение
У больных СРК и СД2 наиболее часто представлены варианты СРК с диареей и СРК с запорами. Кроме того, по сравнению с лицами с СРК, но без диабета у них чаще встречаются варианты СРК-М и СРК-Н, в клинической картине с более высокой частотой встречаются диарея, запоры, абдоминальная боль и вздутие живота, а в анамнезе более часто представлены малоподвижный образ жизни, избыточная масса тела и ожирение, хронический психоэмоциональный стресс, гипотиреоз и перенесенная инфекция COVID-19. При этом данные ФКС и гистологического исследования биоптатов слизистой оболочки толстого кишечника между группами больных СРК с диабетом и без такового практически не различаются.
Полученные в результате исследования данные позволяют констатировать наличие у больных СД2 и СРК ряд значимых клинико-анамнестических особенностей, отличающих их от лиц с СРК без диабета, что следует учитывать при выборе для них оптимальной лечебной тактики.
Вклад авторов. А.Э. Багрий – концепция и дизайн исследования, написание текста. О.Е. Супрун, E.А Андре-ева – сбор и обработка материала. А.А. Евтушенко – статистическая обработка данных. Е.С. Михайличенко, Е.В. Супрун – редактирование.
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы Супрун О.Е. на соискание ученой степени канд. мед. наук: «Синдром раздраженного кишечника у больных с сахарным диабетом 2 типа: диагностика, прогнозирование и лечебные подходы».



